瘢痕不仅影响患者的外观,还可能造成功能障碍、瘙痒或疼痛,对身心健康造成双重负担。传统瘢痕治疗手段如激光、手术切除等虽有一定效果,但对复杂瘢痕(如放射性纤维化、挛缩性瘢痕)的改善有限。近年来,“自体脂肪移植(Autologous Fat Grafting, AFG)”凭借其“体积填充+再生修复”的双重作用,成为瘢痕治疗领域的热点。来自雷根斯堡大学医院整形、手部和重建外科的Dr. Nura Ahmad等人于2024年8月发表在《cells》上的文章《Autologous Fat Grafting—A Panacea for Scar Tissue Therapy?》结合最新研究,系统解析AFG的作用机制、技术要点及临床应用价值。
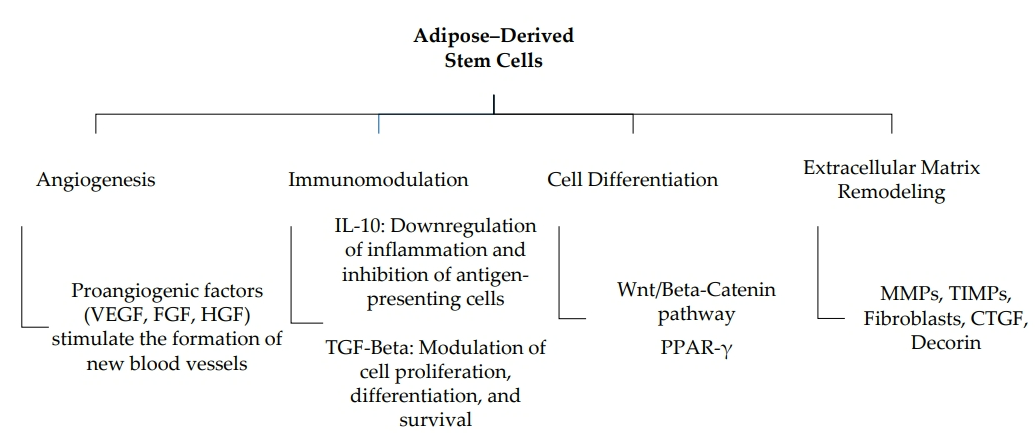
脂肪移植的核心在于脂肪干细胞的再生潜能。
促血管生成:改善瘢痕缺血微环境
免疫调节:打破慢性炎症恶性循环
细胞分化:重建组织功能单元
基质重塑:逆转纤维化进程
ADSCs分泌MMPs(基质金属蛋白酶)降解过度沉积的胶原,同时通过TIMP调控胶原合成与降解的平衡。临床病理显示,移植后瘢痕胶原排列更接近正常皮肤,弹性显著提升。


脂肪获取与处理技术
大颗粒脂肪(>2.4 mm):适用于乳房、臀部等大体积填充,需使用钝针(直径≥2 mm)注射,但栓塞风险较高。 微颗粒脂肪(1.2~2.4 mm):适合精细部位(如眼周、手部),注射更均匀,并发症较少。
纳米脂肪:通过机械乳化过滤获得,富含SVF细胞(每100 mL含190万~300万个活性干细胞),可改善皮肤质地,减少瘢痕色素沉着。
关键工艺:离心与细胞活性保护
离心速度和时间直接影响SVF细胞得率。Baptista团队采用900×g离心15分钟,可保留高活性ADSCs;而酶解法虽细胞得率高,但操作复杂且可能引入外源性风险。最新研究推荐“低速短时离心(如600×g×10分钟)+机械震荡”组合,兼顾效率与安全性。
供区选择:腹部脂肪更具优势?
瘢痕外观与功能评分
采用“患者与观察者瘢痕评估量表(POSAS)”评估显示:
患者评分:疼痛、僵硬、厚度评分改善率达70%~85%,瘙痒改善相对有限(约50%)。
观察者评分:血管分布、色素沉着、弹性等指标提升显著。例如,烧伤后关节挛缩瘢痕经AFG治疗后,关节活动度平均增加30°。
体积与轮廓修复
AFG可有效矫正凹陷性瘢痕(如痤疮瘢痕)和轮廓不平。但脂肪存活率仍是挑战:
短期存活率:约30%~70%,与移植技术密切相关。
提升策略:联合富血小板血浆(PRP)、细胞辅助脂肪移植(CAL)可提高血管化,使存活率稳定在60%以上。
纤维化与疼痛管理
放射性纤维化:AFG通过机械松解+ADSCs分泌CTGF、Decorin,逆转胶原异常沉积。Rigotti团队报道,放疗后胸壁纤维化患者接受AFG后,皮肤溃疡愈合率提升40%。
疼痛缓解:ADSCs分泌BDNF、NGF等神经营养因子,促进神经修复。一项纳入966例患者的Meta分析显示,术后疼痛缓解率达86%,其中乳房切除术后疼痛综合征(PMPS)患者效果最佳。
适应症推荐
凹陷性瘢痕:痤疮瘢痕、创伤性凹陷。
纤维化瘢痕:放射性损伤、烧伤后挛缩。
疼痛性瘢痕:PMPS、剖腹产瘢痕神经痛。
慢性创面:糖尿病足溃疡、静脉性溃疡。
操作要点与风险防控
分层注射:真皮深层与皮下交替注射,避免局部堆积。
单点剂量:每通道注射≤0.1ml,减少脂肪坏死风险。
栓塞预防:避免高压注射,术前超声评估血管走行。
当前局限
证据等级不足:多数研究为小样本回顾性分析,缺乏RCT数据。
评估标准不统一:瘢痕评分工具(如POSAS)主观性强,需结合超声弹性成像、OCT等客观指标。
长期疗效待验证:脂肪存活率随时间下降,需探索冷冻保存、生物支架辅助等新技术。
前沿探索
基因编辑ADSCs:过表达VEGF、IL-10等靶点,增强抗纤维化能力。
联合疗法:AFG+微针、激光可协同促进胶原重塑。
3D打印脂肪组织:构建仿生结构,精准修复复杂缺损。
自体脂肪移植从“单纯填充”迈向“再生修复”,标志着瘢痕治疗进入精准医学时代。未来,随着ADSCs机制研究的深入和生物工程技术的结合,AFG有望成为瘢痕综合管理的基石性手段。临床医生需掌握脂肪处理的核心技术,结合个体化评估,最大化患者获益。











